Sayfa 21/30

Kompleks oluşumu
Kompleks oluşumu çözünürlüğü
etkiler. Önce biraz kompleks iyondan bahsedelim.
Kompleks iyon;
elektron boşluğu olan bazı metallerin, ortaklanmamış
yalnız elektron
çifti içeren
iyon veya moleküllerle oluşturduğu iyondur. Merkez atomu: Merkezde yer alan metaldir. Genellikle geçiş metalleridir.
Geçiş metallerinin
çoğu boş d orbitallerine sahiptir.
Kompleks iyon: Ligandlarla bağ yapmış
metaldir.
Koordinasyon Sayısı: Merkez atomuna bağlı donör
atomları sayısıdır.
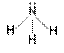
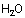
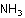
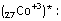
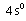
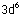


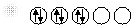
Uyarılmış haldeki Co+3 iyonu ve boş d
orbitalleri
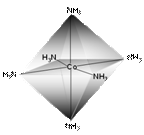
ligand
Merkez atomu

ligand
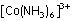
Kompleks iyonu
yalnız elektron çifti içeren donör
atom

ligand
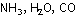
Nötr moleküller
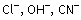
Anyonlar
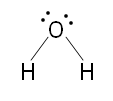
Ligand: Bazı iyonlar ve moleküller ortaklanmamış yalnız elektron
çiftine
sahiptirler ve bu elektronlarını metal atomunun kullanıma sunarlar. Bunlara
ligand denir. Örnek ligandlar:
Donör atom: Ligandı metale bağlayan, yani ortaklanmamış elektron çiftini sunan atoma donör atom denir. Ligandlarda bir veya
birden çok donör atom olabilir. Bunlar birden çok donör atomu ile merkez atomuna bağlanabilir.
(Değerlik ve koordinasyon sayısı farklı
kavramlardır.)
Koordinasyon sayısı 6 dır