Sayfa 23/27


Gazların Yayılma Hızı
Gazların mol kütlesi
azaldıkça yayılma hızı artar.
Sıcaklık arttıkça yayılma
hızı artar.
Hız; mol kütlenin karekökü
ile ters orantılıdır.
Hız; sıcaklığın karekökü ile
doğru orantılıdır.
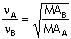
MAA A’nın mol kütlesi, MAB B’nin mol
kütlesi
nA A molekülünün hızı, nB B molekülünün hızı
Diffüzyon, doğada ve vücudumuzda bir çok önemli
olayda yer alır.
Gazların mol kütlesi ile hızı arasındaki ilişki Graham Diffüzyon yasası olarak bilinir.
Diffüzyon; bir gazın başka bir gaz içinde yayılmasıdır.(havada
parfümün yayılması gibi)
Effüzyon; ise kapalı bir kaptaki gazın boşluğa
yayılmasıdır
Her ikisinde hız gazların mol
kütlesinin karekökü ile ters orantılıdır.
Bu konuda yayılma hızı ile yayılma süresi karıştırılmamalı.
Gaz hızlı yayılıyorsa,
yayılması için geçen süre kısa olacaktır.
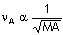
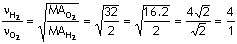
H2 : 2 gr/mol
O2 : 32 gr/mol
H:1 gr/mol, O: 16 gr/mol
(Gaz halde molekül yapısında olurlar. Kütle hesabına dikkat
edin)
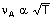
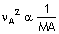
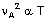
veya
veya
Hidrojen ile oksijenin hızları
arasındaki oran 4/1 imiş. Hidrojen oksijenden 4 kat hızlı.
Hidrojenin hızı
4 iken oksijenin hızı 1 olur.
Hidrojenin 10
sn’de aldığı yolu, oksijen 40 sn de alır.
(hız ile geçen
süre yanıltmasın)