Sayfa 11/31

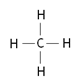

Elementlerin kovalent bağ sayısı yarı dolu orbital sayısı kadardır.
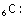
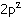
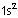
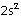
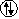

2

4
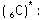
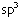
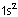

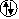

2

4
Temel Hal
Uyarılmış
hal
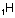
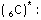
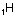
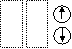
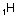
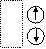
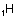

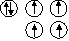
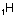
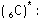
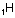
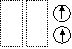
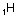
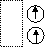
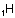

Orbitalleri gösterirken ok yönleri
“spin” i yani elektronların dönme yönünü gösterir. Zıt spinli
elektronlar bir araya gelebilir.
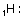
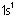

1
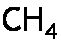
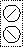

Bu şekilde de karşılaşabilirsiniz
iyonunda olduğu
gibi bazen boş orbitaller ile tam dolu orbitallerin çakışması ile de bağ olur. Bu
“koordinatif bağlar” olarak bilinir. (koordine
bağlar )
Aşağıdaki örnekte bir elektron vererek orbitalini
boşaltan H+ , N’nin 2s orbitali ile örtüşmüştür.
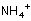
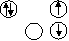
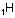
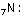
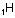

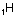


Diğer örnek: Al2Cl6 molekülünde Cl’nin yalnız elektron
çiftlerinin Al’nin boş orbitalleri ile çakışması
sonucu koordinatif bağ oluşur.