Sayfa 9/38


Sistem enerjisini azaltacak, düzensizliğini arttıracak yönde
değişme eğilimindedir.
Endotermik
tepkimelerde girenler minumum enerjili,
Egzotermik
tepkimelerde ürünler minumum enerjilidir.

İyonlarına ayrışma maksimum düzensizliğe
geçiştir. Entropi artar.
Kimyasal tepkimelerde denge; maksimum düzensizlik ile minumum enerji arasındaki uzlaşmanın olduğu durumdur.
Katı > Sıvı > Gaz yönünde değişme, yani
taneciklerin biribirinden uzaklaşması maksimum düzensizlik eğilimine örnektir. Entropi
artar.
Egzotermik
(enerji veren) bir kimyasal tepkime ile yeni bir ürün oluşması, en az enerjili hale geçiştir. Minumum enerjili duruma örnektir.
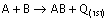
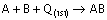
Bir tepkimede minumum enerjili
durum ile maksimum düzensizlik hali aynı yönde veya farklı yönde
olabilir.
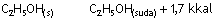
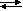
Alkolün suda çözünmesinde minumum enerji ve maksimum düzensizlik ürünler
yönündedir.
1
2
P, V, T aynı, tanecik sayısı n
daha az ise (mol sayısı az) maksimum düzensizlik halidir. Entropi daha
büyüktür. P,T, n aynı V büyük ise düzensizlik artar, Entropi daha büyüktür. T,n, V aynı P
büyük ise düzensizlik artar, Entropi daha büyüktür.
Çözünen iyonların olduğu taraf maksimum
düzensizlik olan taraftır. Entropi daha büyüktür.
Bir sistemin entropisi arttığında çevrenin
entropisi azalır. Sistemin entropisi azaldığında çevrenin entropisi artar.
Isıtma Entropiyi arttırır, soğutma azaltır.
Bir tepkime toplam entropinin daha büyük olduğu
yönde istemlidir.