Sayfa 12/15





Cevap: D
Endotermik (ısı
alan) bir tepkime.
Ürünlerin
mol sayısı daha fazla.



2
1
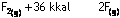
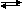
Endotermik (ısı alan) tepkimelerde
sıcaklığı yükseltirsek tepkime ileri çalışır ve ürün derişimi artar.
Sıcaklığı düşürürsek tepkime geri çalışır, ürün derişimi
azalır, girenlerin derişimi artar.
Ürünlerin mol sayısı toplamı ile
girenlerin mol sayısı toplamı farklı. ∆n = 1 Yani ∆n
0’dan farklı. Basınç değişimi dengeyi bozar.
Basınç artarsa
tepkime mol sayısı toplamı daha az olan yöne kayar. Basınç azalırsa, tepkime mol sayısı
toplamı daha çok olan yöne kayar.
Bu tepkimede
basınç düşürülürse tepkime ileri çalışır, ürün derişimi artar.
Basınç yükseltilirse tepkime geri çalışır, girenlerin derişimi artar.
Katalizör tepkimeyi hızlandırır. İleri ve geri tepkimeye aynı
oranda etki eder. Dengeyi bozmaz, denge sabitini de
değiştirmez. Denge derişimlerine etki etmez. Zamandan ve sıcaklıktan
tasarruf sağlar.
Tepkimelerde birden çok koşul göz önüne alınır. Bu soru
için sıcaklık, basınç, hacim değişkenlerinden en uygunu D şıkkıdır.
(…sağdaki cevabın devamı)
Hacim
değişimini basınç’a göre yorumlarız. Hacmin değişmesi basıncı değiştirir.
Hacim azaldıkça
basınç artar, hacim arttıkça basınç azalır.
Bu tepkimede
hacmi küçültmek basıncı arttırır, tepkime geri kayar, girenlerin derişimi artar. Hacmi büyütmek
basıncı düşürür, tepkime ileri kayar, ürün derişimi artar...devamı
Sıcaklığın,
basıncın ve hacmin etkisi
Le Chatelier
ilkesine göre düşünülür.